| 好文 | 您所在的位置:网站首页 › fxr抑制剂 › 好文 |
好文
|
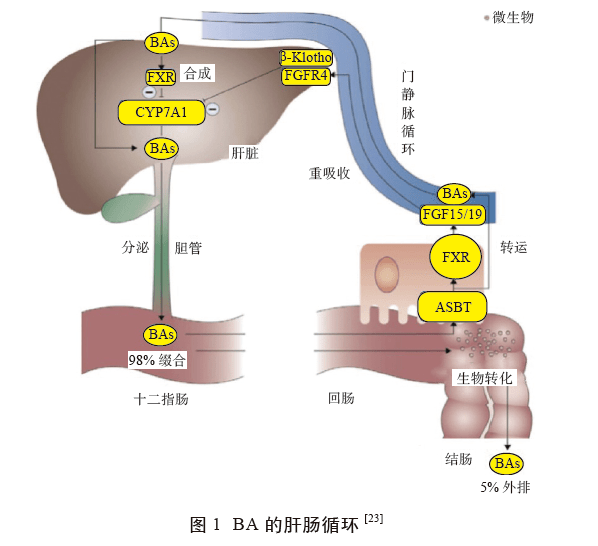
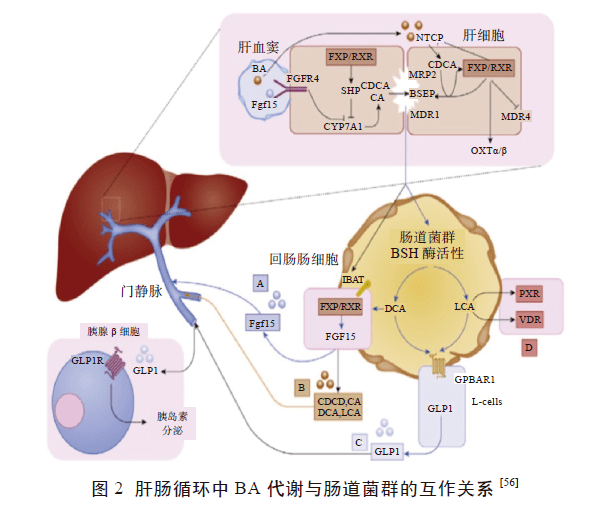
1.2 BA 相关受体及信号通路 BA是代谢途径网络的关键调节因子,在肝脏和肠道基因表达中起关键作用,并且直接参与复杂的代谢网络,通过激活在不同细胞类型中表达的特异性受体来引发BA的生理作用,进而调节生物的代谢,从而触发细胞信号传导途径。BA是FXR、FGFR4 和TGR5等受体的有效配体,通过这些受体的作用可以产生非基因组效应。 1.2.1 BA介导的FXR 信号通路 FXR 是参与调节BA的肠肝循环和BA 生物合成最重要的受体,其在肝脏、肠道、肾脏等组织中高水平表达。BA 是FXR 受体最有效的内源性配体,而FXR 受体也是肝脏合成BA 的抑制剂,在肝肠循环BA 代谢过程中起重要的调节作用,能有效控制肝脏和肠道中BA 含量。在肝脏中,活化后的FXR 通过诱导小异二聚体配偶体(SmallHeterodimer Partner,SHP)调节核孤儿受体肝脏相关同系物1(Liver Related Homologue-1, LRH-1 ) 基因的表达,激活FXR-SHP 信号通路,间接影响BA的分泌,进而影响BA的合成、转运等。 Murashita 等研究发现,虹鳟(Oncorhynchus mykiss )肝脏中的SHP可通过抑制CYP7A1 和CYP8B1 基因的表达来抑制BA合成; Modica等研究也表明,FXR 可诱导SHP,抑制LRH-1 的转录和CYP7A1 的表达,进而影响BA合成的负反馈调节。 在肠道中,BA 刺激FXR 受体,激活FXR-FGF15/19 信号通路,介导肠上皮细胞内成纤维细胞生长因子(Fibroblast Growth Factor,FGF15/19)的表达进而影响细胞表面FGFR4 受体(Fibroblast Growth FactorReceptors 4,FGFR4) 的分泌, 从而抑制CYP7A1、CYP8B1 等的表达,最终维持机体内BA 的代谢稳态。 Kong等研究表明,FXR 可影响肠道内FGF15 的表达水平进而抑制CYP7A1 的转录,从而影响BA的合成量,证明FXR-FGF15/19 信号通路可在修复肝肠胆相关疾病的过程中发挥重要作用。综上,FXR 在肝脏与肠道中的2条信号通路协同,也表明肝和肠中的FXR基因之间存在密不可分的协作关系。Song等研究报道,BA 可激活FXR 并增加SHP 和FGF15 的mRNA 表达量,并且认为CA 和DCA 比CDCA 和LCA 作为FXR的激动剂效果更好。同样,多篇文献也报道了CDCA是FXR 最有效的体外激动剂。 1.2.2 BA 介导的FGFR4信号通路 FGFR4 是一类跨膜高亲和力酪氨酸激酶受体,通过与FGF15/19 结合来介导FGF 信号传递到细胞质中。有研究称,FGF15/19-FGFR4 信号通路的激活,有助于增加多种细胞的增殖并减少细胞凋亡。FGF15/19 是FGF 分泌信号分子家族的成员,是一大类生长因子,涉及多种生物反应,尤其在BA生理过程中起着至关重要的作用。 目前,已知鼠FGF15 和人类(以及斑马鱼)FGF19 在氨基酸水平上的同源性相对较高,因此FGF15 与FGF19 为具有相似功能的同源基因。有研究表明,FXR 经BA 刺激后介导FGF15/19 的表达,激活其受体FGFR4 的分泌后,会触发肝细胞中ERK1/2 和JNK 信号通路,从而抑制CYP7A1 和YP7B1 的表达,最终影响BA 的生物合成。此外,也有研究认为,FGFR4 的激活会触发磷脂酰肌醇-3 激酶(Phosphatidylinositol 3-Kinase,PI3K)信号通路,抑制叉头框蛋白O1(FoxO1 )的表达,进而抑制CYP7A1 的转录。 1.2.3 BA 介导的TGR5 信号通路 TGR5 也称为G蛋白偶联的BA受体1(GPBAR1),是BA 的G 蛋白偶联的膜受体,最初鉴定于2002年,在肝脏、脾脏、肾脏、肠道和胆囊等组织及巨噬细胞中广泛表达。BA 是TGR5受体最有效的配体,可以直接激活或调节几种G蛋白偶联受体(GPCR)的信号传导,其具有多种生理调节功能,主要在促进脂肪分解、葡萄糖稳态和能量消耗等方面发挥关键作用。 有研究表明,TGR5的激活会触发p38丝裂原活化蛋白激酶(Mitogen-Activated ProteinKinases,p38MAPK)信号通路,活化ERK1/2 和JNK,增加NF-κB、IL-6 和TNF-α 的表达量,发挥免疫功能。 ● 2 肠道微生态● 肠道微生态系统在动物机体中占主要位置,同时也十分复杂,在维持动物体内正常营养代谢、增强机体免疫功能及免受外来物质侵袭等方面发挥至关重要的作用,一旦发生失调,会直接影响肠道免疫系统的发育并影响宿主代谢,直接或间接地引发多种疾病。肠道菌群在整个肠道微生态系统中占核心位置,通过为宿主提供必需化合物,在参与BA 的生物合成、能量及糖脂代谢、促进营养物质的消化和吸收、调节宿主免疫功能以及保护宿主免受外界毒害物质的侵袭等多方面发挥关键作用。 肠道菌群的主要功能包括对机体营养作用、免疫作用及生物屏障作用等。有报道称,肠道菌群的代谢产物(如氧化三甲胺、短链脂肪酸等)均可影响肠道屏障功能、糖脂代谢。动物肠道菌群主要由乳杆菌属(Lactobacillus)、链球菌属(Streptococcus)和葡萄球菌属(Staphylococcus)等组成,其次为肠杆菌属(Enterobacteria)、肠球菌属(Enterococcus)、拟杆菌属(Bacteroides) 和梭菌属(Clostridium) 等。 肠道菌群的组成可通过多种方法检测,目前常用的主要是16S RNA 和宏基因组测序,此外还有分离培养、代谢组学及质谱技术等。近年来,肠道菌群的主要调节剂包括益生菌、抗菌肽、中草药及植物提取物等。无可否认,在畜牧产业中,抗生素对肠道菌群也有一定的调节作用,在促进动物生长及防治疾病等方面发挥积极作用,但抗生素的耐药性和药物残留等问题无法得到解决,正逐步退出畜牧业。在调节动物肠道菌群中,常用的益生菌主要仍集中于乳酸菌和芽孢杆菌及中草药(人参、黄岑等)、植物提取物(如人参多糖、猴头菇多糖等)。此外,抗菌肽是核糖体合成的天然抗生素,细菌、植物及动物等生物均能产生抗菌肽,其主要功能是调节肠道菌群的数量和组成,且与肠道菌群具有双向调控作用。 ● 3 BA 代谢与肠道微生态的互作关系● BA代谢与肠道菌群之间存在密切相关的互作关系(图2),BA会通过自身的生理作用及其所介导的信号通路来影响肠道菌群的数量和组成,而肠道菌群数量及组成的变化也会影响BA的代谢,还可激活BA相关信号通路调控BA代谢,二者之间的互作关系会造成相同影响,即引发动物肝肠胆相关疾病。
3.1 BA对肠道菌群的调节作用 BA在肠道中主要通过Bacteroides 、真杆菌属(Eubacterium)、Clostridium和Lactobacillus 的厌氧作用进行生物转化,与牛磺酸和甘氨酸结合后通过胆盐水解酶(Bile Salt Hydrolase,BSH)催化共轭BA的解偶联,恢复成未结合的游离胆汁酸。BSH是肠道菌群产生的一种酶,可影响BA发挥不同的生理功能,不同的BSH可能对不同的BA组成有反应,BSH 可能具有解毒作用,BA去缀合也由具有BSH活性的肠道微生物进行,进而改善哺乳动物肠道菌群的定植。Phylum Firmicutes是将初级胆汁酸去共轭和脱羟基成为次级胆汁酸的主要细菌,粪便中外排的BA减少会引起肠道中的Phylum Firmicutes发生改变。 Kusumotoa等研究表明,添加BA结合树脂(Bile Acid Binding Resin,BAR)改变了肠道菌群的组成,增加了Phylum Firmicutes 并减少了Bacteroides数量,进而降低了脂肪沉积。 BAR是肠道中能够降低血清胆固醇的BA,可引起肠道菌群的变化,并增加丙酸的产生量,可有效改善对葡萄糖的耐受性不良并预防人和动物的肥胖、脂肪肝等疾病。此外,BA 可降低肠道菌群代谢物短链脂肪酸(SCFA)的产量,且具有抑菌活性,能有效抑制肠道病原菌的生长增殖,并且通过FXR 诱导的抗菌肽具有间接作用。 Peng 等给草鱼(Ctenopharyngodon idella ) 饲喂BA 50 d, 发现Lactobacillus 和双歧杆菌(Bifidobacterium )等有益菌数量增加,气单胞菌和大肠杆菌等有害菌数量减少。 BA 可作为信号分子调节肠道菌群的生理功能,FXR 受体与肠道中的免疫调节和屏障功能有关。Stenman 等研究表明,BA 生成量增加导致肠道中FXR 表达的增加,引起肠道菌群的变化,进而调节肠道屏障功能。 3.2 肠道微生态对BA 的调节作用 在肠道中,初级胆汁酸的复杂代谢主要受肠道菌群的调节,BA组成发生改变,使得肠道菌群在调节动物机体代谢方面具有重要作用。BA池的大小和组成与肠道菌群密切相关,某些特定的肠道菌群组成可能导致BA 池发生明显变化。BA主要转化方式包括C3、C7 和C12 上羟基的去共轭、氧化和差向异构化、7-脱羟基化、酯化和脱硫等(表1)。 大量研究表明,动物肠道内的正常菌群会通过水解酶和羟基的氧化共同作用,来解离BA 中的甘氨酸或牛磺酸。肠道菌群的存在增加了胆汁酸池的疏水性,不同的肠道菌群组成产生了不同的BA谱。
3.3 肠道微生态对BA 代谢的调节作用 肠道菌群是有效的FXR 活化剂。Sayin 研究证实,常规饲养小鼠中的MCA 水平显著降低,而无菌的FXR 缺失型小鼠BA水平升高,肠道菌群通过FXR 调节肠道中FGF15和肝脏中CYP7A1 的表达,进而抑制BA 的合成和代谢。已知,益生菌是改善肠道菌群组成、调节肠道菌群平衡的最有效的调节剂,不同的益生菌水解特定的BA底物。有研究表明,益生菌代谢产物能够调节肠道中FXR、维生素D 受体和过氧化物酶体增殖物激活受体(PPARs)的表达。 Degirolamo 等研究发现,VSL#3 复合益生菌(Lactobacillus、Bifidobacterium 和Streptococcus thermophilus )能够有效调节小鼠的肠道菌群的组成,Phylum Firmicutes 和放线菌属(Actinomyces )数量显著增加,Bacteroides 和变形杆菌属(Proteus)数量下降,进而导致肠道中FXR 和FGF15 表达下调,促进CYP7A1 和CYP8B1 的表达,调节肝脏中BA 的新合成。 Liu 等研究发现,有机氯农药使小鼠肠道菌群的相对丰度和组成发生改变后,Lactobacillus 数量及BSH 活性均有所减少,而后导致BA组成发生变化,疏水性增强,相关基因的表达下降,最终影响了肝脏和肠道BA的分布和代谢。 这些研究均表明,肠道菌群能够通过胆汁酸受体及其所介导的信号通路来影响BA的代谢,肠道菌群一旦失调随即会产生BA 代谢障碍,引发肠炎、脂肪肝、胆囊肿大等疾病。 ● 4 小结与展望● BA 作为关键的信号分子与其相关受体结合后调节BA、葡萄糖、脂类和能量代谢,BA代谢与肠道菌群之间存在密切相关的互作关系,且二者与动物机体之间也呈现“三角动态平衡”状态。BA 会通过自身的生理作用机制及其所激活的FXR-FGF15/19等通路对肠道菌群的数量及组成进行影响,反之肠道菌群也会通过所产生的BSH 等酶的作用影响肠道中BA 的合成、代谢,同时肠道菌群还可激活BA 的FXR-FGF15/19、FXR-SHP等信号通路调控BA 代谢。益生菌能有效改善肠道菌群组成,维持肠道微生态平衡,今后有望通过益生菌调节动物肠道菌群以影响BA代谢,进而维持肝肠循环稳态,最终实现对动物肝肠胆相关疾病的防治。与此同时,本课题组将继续深入研究BA代谢与肠道微生态之间的双向调控机制,进一步探寻肠道菌群-BA代谢之间的互作关系及其对动物机体的影响。(完)
点分享
点点赞
点在看 返回搜狐,查看更多 |
【本文地址】