| 四羰基合镍为什么是四面体构型,不是正方形? | 您所在的位置:网站首页 › ch3空间构型 › 四羰基合镍为什么是四面体构型,不是正方形? |
四羰基合镍为什么是四面体构型,不是正方形?
|
已经有了价键理论解释和晶体场的解释,那说个其他的吧。这个确实和电子数有关,最常见的平面四边形构型的配合物,比如顺铂,是16电子的镍和铂系金属配合物。这个d¹⁰,18电子的配合物很难形成平面四边形的构型。 下图是平面ML₄的轨道作用图,其中的1b₁g和2b₁g轨道是d x²-y²的配体的形成的成键和反键轨道,很明显两者形成“很强”的键。填入16个电子时能量很高的2b1g是空出来的,对平面的构型有利,而18电子时这个反键轨道就要填电子了,。  Orbital interaction diagram for asquare planar, D4h ML4 complex,Orbital Interactions in Chemistry, Second Edition Orbital interaction diagram for asquare planar, D4h ML4 complex,Orbital Interactions in Chemistry, Second Edition在反映不同结构轨道能量变化的Walsh图中,这个变化更加明显。左边是D4h 的平面正方形构型,右边是正四面体构型,填入18个电子时右边的构型更有利。因为L是氢,下图的结果接近晶体场,右边正四面体构型中最上面的两个轨道就对应晶体场理论中正四面体场d轨道分裂出的的t₂(dxy dyz dxz)和e(dz² dx²-y²)。 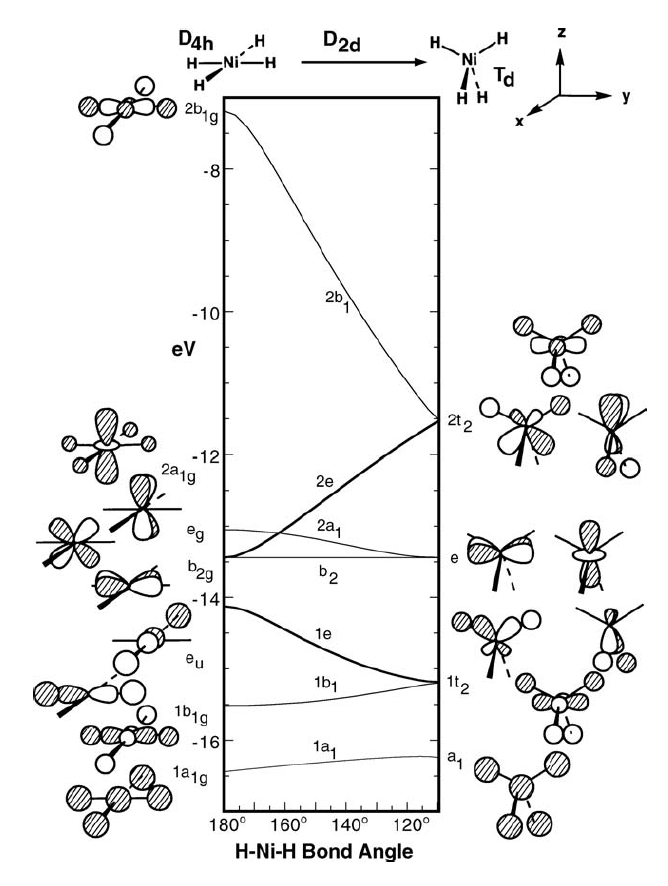 上面的讨论没有涉及配体,引入CO配体后轨道的能量和H有不同。下面是理论计算的结果,CO作为能形成反馈π键的配体,CO的反键轨道和dy |
【本文地址】
公司简介
联系我们